jueves, 21 de agosto de 2008
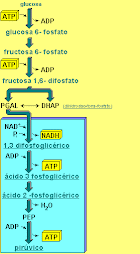
Más sobre glucólisis
Este sitio es interesante y completo. Los temas están bien abordados. Lo recomiendo como introducción
martes, 19 de agosto de 2008
lunes, 18 de agosto de 2008
Azúcares reductores
Los azucares reductores, provocan la alteración de las proteínas mediante la reacción de glucosilación no enzimática también denominada reacción de Maillard o glicación. Esta reacción se produce en varias etapas: las iniciales son reversibles y se completan en tiempos relativamente cortos, mientras que las posteriores transcurren más lentamente y son irreversibles. Se postula que tanto las etapas iniciales como las finales de la glucosilación están implicadas en los procesos de envejecimiento celular y en el desarrollo de las complicaciones crónicas de la diabetes.
La glucosa es el azúcar reductor más abundante en el organismo. Su concentración en la sangre está sometida a un cuidadoso mecanismo de regulación en individuos sanos y, en personas que padecen diabetes, aumenta sustancialmente. Esto lleva a que éste sea el azúcar reductor generalmente considerado en las reacciones de glucosilación no enzimática de interés biológico. Sin embargo, cualquier azúcar que posea un grupo carbonilo libre puede reaccionar con los grupos amino primarios de las proteínas para formar bases de Schiff. La reactividad de los distintos azúcares está dada por la disponibilidad de su grupo carbonilo. Se sabe que la forma abierta o extendida de los azúcares no es muy estable, a tal punto que, por ejemplo, en la glucosa representa sólo el 0,002 %. Las moléculas de azúcar consiguen estabilizarse a través de un equilibrio entre dicha forma abierta y por lo menos dos formas cerradas (anómeros cíclicos) en las que el grupo carbonilo ha desaparecido. En 1953, el grupo de Aaron Katchalsky, en el entonces recientemente creado Instituto Weizmann de Israel, demostró que existe una correlación entre la velocidad de la reacción de glicación y la proporción de la forma abierta de cada azúcar [Katchalsky & Sharon, 1953]. De hecho, los azúcares fosfato, que son azúcares reductores de gran importancia en el interior celular, poseen mayor capacidad glucosilante que la glucosa dada su mayor proporción de forma carbonílica (abierta).La sacarosa es un disacárido que no posee carbonos anoméricos libres por lo que carece de poder reductor y la reacción con el licor de Fehling es negativa.
La glucosa es el azúcar reductor más abundante en el organismo. Su concentración en la sangre está sometida a un cuidadoso mecanismo de regulación en individuos sanos y, en personas que padecen diabetes, aumenta sustancialmente. Esto lleva a que éste sea el azúcar reductor generalmente considerado en las reacciones de glucosilación no enzimática de interés biológico. Sin embargo, cualquier azúcar que posea un grupo carbonilo libre puede reaccionar con los grupos amino primarios de las proteínas para formar bases de Schiff. La reactividad de los distintos azúcares está dada por la disponibilidad de su grupo carbonilo. Se sabe que la forma abierta o extendida de los azúcares no es muy estable, a tal punto que, por ejemplo, en la glucosa representa sólo el 0,002 %. Las moléculas de azúcar consiguen estabilizarse a través de un equilibrio entre dicha forma abierta y por lo menos dos formas cerradas (anómeros cíclicos) en las que el grupo carbonilo ha desaparecido. En 1953, el grupo de Aaron Katchalsky, en el entonces recientemente creado Instituto Weizmann de Israel, demostró que existe una correlación entre la velocidad de la reacción de glicación y la proporción de la forma abierta de cada azúcar [Katchalsky & Sharon, 1953]. De hecho, los azúcares fosfato, que son azúcares reductores de gran importancia en el interior celular, poseen mayor capacidad glucosilante que la glucosa dada su mayor proporción de forma carbonílica (abierta).La sacarosa es un disacárido que no posee carbonos anoméricos libres por lo que carece de poder reductor y la reacción con el licor de Fehling es negativa.
HIDRATOS DE CARBONO
1. Definición y clasificación
Los carbohidratos o sacáridos (del griego: sakcharón, azúcar) son compuestos esenciales de los organismos vivos y son la clase más abundante de moléculas biológicas. El nombre carbohidratos significa literalmente hidratos de carbono y proviene de su composición química, que para muchos de ellos es (C·H2O)n , donde n ³3. Es decir, son compuestos en los que n átomos de carbono parecen estar hidratados con n moléculas de agua. En realidad se trata de polihidroxialdehidos y polihidrohicetonas (y algunos derivados de éstos), cadenas de carbono que contienen un grupo aldehído o cetónico y varios grupos hidroxilos
Las unidades básicas de los carbohidratos son los monosacáridos, no hidrolizables en unidades más pequeñas. La glucosa es el monosacárido más abundante; tiene 6 átomos de carbono y es el combustible principal para la mayoría de los organismos. Los oligosacáridos contienen de dos a diez unidades de monosacáridos unidas covalentemente. Por su parte, los polisacáridos están constituidos por gran número de unidades de monosacáridos unidos covalentemente, alcanzando pesos moleculares de hasta 106 dalton (g/mol). Los polisacáridos desempeñan dos funciones biológicas principales: algunos almacenan energía metabólica y otros sirven de elementos estructurales a la célula.
2. Monosacáridos
Los monosacáridos se clasifican según la naturaleza química de su grupo carbonilo y del número de átomos de carbono que poseen.
Atendiendo a la naturaleza química del grupo funcional carbonílico, si éste es aldehído el monosacárido recibe el nombre genérico de aldosa, y si es cetónico el monosacárido se le designa como cetosa. Dependiendo del número de átomos de carbono de la molécula, los monosacáridos se denominan triosas, tetrosas, pentosas, hexosas, etc. cuando contienen tres, cuatro, cinco, seis, etc. átomos de carbono. Se conocen en la naturaleza monosacáridos de hasta 8 átomos de carbono.
La combinación de ambas nomenclaturas anteriores permite denominar con el término aldohexosa a un azúcar (-osa) de seis átomos de carbono (-hex-), cuyo carbono carbonílico es una aldosa (aldo-). Por ejemplo, la glucosa.
El gliceraldehido es la aldosa más simple. Está formado por tres átomos de carbono, el primero contiene el grupo aldehído, el segundo tiene unido un hidrógeno y un grupo hidroxilo, mientras que el tercero posee dos hidrógenos y un hidroxilo. De los tres carbonos, el segundo (C-2) posee los cuatros sustituyentes distintos y por esta característica recibe el nombre de carbono asimétrico o quiral. Este hecho hace que el gliceraldehido exista en dos estructuras espaciales que se diferencian por cierta propiedad física (actividad óptica): una tiene el hidroxilo del C-2 hacia la derecha (D-gliceraldehido) y la otra posee el hidroxilo del C-2 hacia la izquierda (L-gliceradehido).
Los Disacáridos
Son dímeros formados por dos moléculas de monosacáridos, iguales o diferentes, unidas mediante enlace glucosídico. Este enlace puede realizarse de dos formas distintas; tomemos como ejemplo la glucosa.
Polisacáridos
Son polímeros de monosacáridos unidos por enlace O-glucosídico. Entre los polímeros naturales, algunos de los más abundantes y de mayor significativo biológico son el almidón, el glucógeno y la celulosa. Los tres están formados por moléculas de D-glucosa y sólo se diferencian en el tipo de enlace glucosídico, constituyendo estructuras espaciales diferentes.
El almidón
Es la principal reserva de hidratos de carbono que sintetizan las plantas y es también la principal fuente de glucosa para la alimentación de los animales. Está formado por una mezcla de dos polisacáridos, la amilosa (en un 20 %) y la amilopectina (en un 80 %).
El Glucógeno
El glucógeno es el polisacárido de reserva de glucosa en los animales y constituye el equivalente al almidón en las células vegetales. Se halla presente en todas las células, aunque preferentemente se acumula en los músculos esqueléticos y especialmente en el hígado (10 % en peso), en cuyas células el glucógeno aparece en forma de grandes gránulos. La estructura principal del glucógeno se parece a la amilopectina, posee una cadena líneal con uniones a-(1-4) y ramificaciones a-(1-6), aunque en este caso aparecen cada 8 ó 12 unidades de glucosa
Los carbohidratos o sacáridos (del griego: sakcharón, azúcar) son compuestos esenciales de los organismos vivos y son la clase más abundante de moléculas biológicas. El nombre carbohidratos significa literalmente hidratos de carbono y proviene de su composición química, que para muchos de ellos es (C·H2O)n , donde n ³3. Es decir, son compuestos en los que n átomos de carbono parecen estar hidratados con n moléculas de agua. En realidad se trata de polihidroxialdehidos y polihidrohicetonas (y algunos derivados de éstos), cadenas de carbono que contienen un grupo aldehído o cetónico y varios grupos hidroxilos
Las unidades básicas de los carbohidratos son los monosacáridos, no hidrolizables en unidades más pequeñas. La glucosa es el monosacárido más abundante; tiene 6 átomos de carbono y es el combustible principal para la mayoría de los organismos. Los oligosacáridos contienen de dos a diez unidades de monosacáridos unidas covalentemente. Por su parte, los polisacáridos están constituidos por gran número de unidades de monosacáridos unidos covalentemente, alcanzando pesos moleculares de hasta 106 dalton (g/mol). Los polisacáridos desempeñan dos funciones biológicas principales: algunos almacenan energía metabólica y otros sirven de elementos estructurales a la célula.
2. Monosacáridos
Los monosacáridos se clasifican según la naturaleza química de su grupo carbonilo y del número de átomos de carbono que poseen.
Atendiendo a la naturaleza química del grupo funcional carbonílico, si éste es aldehído el monosacárido recibe el nombre genérico de aldosa, y si es cetónico el monosacárido se le designa como cetosa. Dependiendo del número de átomos de carbono de la molécula, los monosacáridos se denominan triosas, tetrosas, pentosas, hexosas, etc. cuando contienen tres, cuatro, cinco, seis, etc. átomos de carbono. Se conocen en la naturaleza monosacáridos de hasta 8 átomos de carbono.
La combinación de ambas nomenclaturas anteriores permite denominar con el término aldohexosa a un azúcar (-osa) de seis átomos de carbono (-hex-), cuyo carbono carbonílico es una aldosa (aldo-). Por ejemplo, la glucosa.
El gliceraldehido es la aldosa más simple. Está formado por tres átomos de carbono, el primero contiene el grupo aldehído, el segundo tiene unido un hidrógeno y un grupo hidroxilo, mientras que el tercero posee dos hidrógenos y un hidroxilo. De los tres carbonos, el segundo (C-2) posee los cuatros sustituyentes distintos y por esta característica recibe el nombre de carbono asimétrico o quiral. Este hecho hace que el gliceraldehido exista en dos estructuras espaciales que se diferencian por cierta propiedad física (actividad óptica): una tiene el hidroxilo del C-2 hacia la derecha (D-gliceraldehido) y la otra posee el hidroxilo del C-2 hacia la izquierda (L-gliceradehido).
Los Disacáridos
Son dímeros formados por dos moléculas de monosacáridos, iguales o diferentes, unidas mediante enlace glucosídico. Este enlace puede realizarse de dos formas distintas; tomemos como ejemplo la glucosa.
Polisacáridos
Son polímeros de monosacáridos unidos por enlace O-glucosídico. Entre los polímeros naturales, algunos de los más abundantes y de mayor significativo biológico son el almidón, el glucógeno y la celulosa. Los tres están formados por moléculas de D-glucosa y sólo se diferencian en el tipo de enlace glucosídico, constituyendo estructuras espaciales diferentes.
El almidón
Es la principal reserva de hidratos de carbono que sintetizan las plantas y es también la principal fuente de glucosa para la alimentación de los animales. Está formado por una mezcla de dos polisacáridos, la amilosa (en un 20 %) y la amilopectina (en un 80 %).
El Glucógeno
El glucógeno es el polisacárido de reserva de glucosa en los animales y constituye el equivalente al almidón en las células vegetales. Se halla presente en todas las células, aunque preferentemente se acumula en los músculos esqueléticos y especialmente en el hígado (10 % en peso), en cuyas células el glucógeno aparece en forma de grandes gránulos. La estructura principal del glucógeno se parece a la amilopectina, posee una cadena líneal con uniones a-(1-4) y ramificaciones a-(1-6), aunque en este caso aparecen cada 8 ó 12 unidades de glucosa
VITAMINAS
Son sustancias orgánicas, de naturaleza y composición variada.
Se necesitan en pequeñas cantidades, aunque su presencia es imprescindible para el desarrollo normal del organismo.
Las necesidades vitamínicas varian según las especies, con la edad y con la actividad.
Los vegetales, hongos y microorganismos son capaces de elaborarlas por sí mismos. Los animales, salvo algunas excepciones, carecen de esta capacidad, por lo que deben obtenerlas a partir de los alimentos de la dieta. En algunos casos los animales obtienen algunas vitaminas a través de sus paredes intestinales, cuya flora bacteriana simbionte las producen.
Ciertas vitaminas son ingeridas como provitaminas (inactivas) y posteriormente el metabolismo animal las transforma en activas (en el intestino, en el el hígado, en la piel, etc..), trás alguna modificación en sus moléculas.
Son sustancias lábiles, ya que se alteran facilmente por cambios de temperatura y pH, y también por almacenamientos prolongados.
Las vitaminas se designan utilizando letras mayúsculas, el nombre de la enfermedad que ocasiona su carencia o bien el nombre de su constitución química.
Clásicamente se establecen 2 grupos según su capacidad de disolución en agua o en las grasas o disolventes de éstas. Así, se habla de: vitaminas hidrosolubles y liposolubles respectivamente.
a) Vitaminas Liposolubles
Son vitaminas no solubles en agua y químicamente se trata de lípidos insaponificables, caracterizados por su incapacidad para formar jabones, ya que carecen en sus moléculas de ácidos grasos unidos mediante enlaces éster.
Encontramos las siguientes:
· VITAMINA A. Retinol. Antixeroftálmica.
· VITAMINA E. Tocoferol. Antiestéril.
· VITAMINA K. Naftoquinona. Antihemorrágica.
· VITAMINA D. Calciferol. Antirraquítica.
b) Vitaminas Hidrosolubles
Vitamina B1
Se necesitan en pequeñas cantidades, aunque su presencia es imprescindible para el desarrollo normal del organismo.
Las necesidades vitamínicas varian según las especies, con la edad y con la actividad.
Los vegetales, hongos y microorganismos son capaces de elaborarlas por sí mismos. Los animales, salvo algunas excepciones, carecen de esta capacidad, por lo que deben obtenerlas a partir de los alimentos de la dieta. En algunos casos los animales obtienen algunas vitaminas a través de sus paredes intestinales, cuya flora bacteriana simbionte las producen.
Ciertas vitaminas son ingeridas como provitaminas (inactivas) y posteriormente el metabolismo animal las transforma en activas (en el intestino, en el el hígado, en la piel, etc..), trás alguna modificación en sus moléculas.
Son sustancias lábiles, ya que se alteran facilmente por cambios de temperatura y pH, y también por almacenamientos prolongados.
Las vitaminas se designan utilizando letras mayúsculas, el nombre de la enfermedad que ocasiona su carencia o bien el nombre de su constitución química.
Clásicamente se establecen 2 grupos según su capacidad de disolución en agua o en las grasas o disolventes de éstas. Así, se habla de: vitaminas hidrosolubles y liposolubles respectivamente.
a) Vitaminas Liposolubles
Son vitaminas no solubles en agua y químicamente se trata de lípidos insaponificables, caracterizados por su incapacidad para formar jabones, ya que carecen en sus moléculas de ácidos grasos unidos mediante enlaces éster.
Encontramos las siguientes:
· VITAMINA A. Retinol. Antixeroftálmica.
· VITAMINA E. Tocoferol. Antiestéril.
· VITAMINA K. Naftoquinona. Antihemorrágica.
· VITAMINA D. Calciferol. Antirraquítica.
b) Vitaminas Hidrosolubles
Vitamina B1
PROTEINAS
Las proteínas son cadenas polipéptidicas que se diferencian de los oligopéptidos en el número de aminoácidos que contienen, en su carácter funcional y sobre todo en que son el resultado del proceso de traducción genética. La conformación de una proteína hace referencia a la disposición espacial de la misma, aspecto de vital importancia, pues va a estar directamente relacionado con la función que desempeñan. Según la conformación las proteínas pueden clasificarse en fibrosas y globulares.
Las fibrosas poseen las cadenas polipeptídicas ordenadas de modo paralelo a lo largo de un eje. Forman materiales físicamente resistentes e insolubles en agua, siendo elementos básicamente estructurales como por ejemplo la a-queratina del pelo, la fibroina de la seda o el colágeno de los tendones.
Por su parte, las proteínas globulares, están constituidas por una o varias cadenas polipeptídicas plegadas de modo que puedan adoptar una conformación esférica o globular, desempeñando diferentes funciones de tipo metabólico (proteínas transportadoras, enzimas, anticuerpos,...). Algunas proteínas incluso pueden situarse entre estas dos conformaciones como sería el caso de la miosina de los músculos o el fibrinógeno de la sangre.
Las proteínas se clasifican en dos grandes grupos
· Proteínas simples
· Proteínas conjugadas
Proteínas simples: son aquellas que por hidrólisis solo dan origen a aa. Pueden estar formadas por más de una cadena polipeptídica, por ejemplo albúminas, globulinas, histonas, glutelinas, escleroproteínas como queratina, colágeno, elastinas.Proteínas conjugadas: formadas por asociación de una proteína simple y una porción no proteica integrando una unidad molecular. Corrientemente se llama apoproteína a la porción proteica, mientras que la otra porción se denomina grupo prostético
La conformación que presenta una proteína va a depender directamente de los distintos niveles estructurales (hasta cuatro) que posee:
a) Estructura primaria: hace referencia a la posición que ocupa cada aminoácido en la cadena polipeptídica, es decir nos da idea de la secuencia de la proteína. La importancia de este nivel radica en que la posición que ocupa cada aminoácido dentro de la cadena va a condicionar enormemente el resto de los niveles estructurales y en último término la función que desempeña la proteína.
b) Estructura secundaria: hace referencia a la ordenación regular y periódica de la cadena polipeptídica en una dirección determinada. Básicamente, podemos encontrar dos tipos de estructura secundaria, la hélice-a y la conformación-ß.
En la Hélice-a (Fig.8) la cadena polipeptídica adopta una conformación helicoidal. Las estructuras helicoidales se caracterizan por el numero de aminoácidos por vuelta (n) y por su paso de rosca (p), o distancia entre vueltas. Esta conformación se estabiliza por puentes de hidrógeno (R-C=O ····· H-N-R) intracatenarios (dentro de la hélice). Además, los restos -R de los aminoácidos se disponen hacia fuera de la hélice evitando las interacciones estéricas (por grupos voluminosos) y estabilizando la conformación. Por otro lado, la hélice-a se distorsiona o pierde la conformación cuando en la secuencia aparece una prolina, único aminoácido ciclado por su grupo a-amino.
En la conformación-ß la cadena adopta una ordenación lineal en la que los restos -R, de los aminoácidos, se van alternando por encima y por debajo (zig-zag) del plano del enlace peptídico. Esta conformación se estabiliza con puentes de hidrógeno entre varias cadenas de proteínas con conformación-ß. El resultado de estas interacciones es la hoja plegada ß, que puede presentar un plegamiento paralelo, (en el que las cadenas vecinas se desarrollan en la misma dirección), o bien un plegamiento antiparalelo con cadenas vecinas en direcciones opuestas.
c)Estructura terciaria : hace referencia al modo en que se curvan o pliegan en el espacio los segmentos de hélice-a y/o conformación-ß, que presenta una cadena polipeptídica de los proteínas globulares.
d) Estructura cuaternaria: Muchas proteínas globulares son oligoméricas, es decir están formadas por más de una subunidad polipeptídica. La posición espacial que ocupa cada una de estas subunidades respecto a las otras queda determinada por la estructura cuaternaria.
Las fibrosas poseen las cadenas polipeptídicas ordenadas de modo paralelo a lo largo de un eje. Forman materiales físicamente resistentes e insolubles en agua, siendo elementos básicamente estructurales como por ejemplo la a-queratina del pelo, la fibroina de la seda o el colágeno de los tendones.
Por su parte, las proteínas globulares, están constituidas por una o varias cadenas polipeptídicas plegadas de modo que puedan adoptar una conformación esférica o globular, desempeñando diferentes funciones de tipo metabólico (proteínas transportadoras, enzimas, anticuerpos,...). Algunas proteínas incluso pueden situarse entre estas dos conformaciones como sería el caso de la miosina de los músculos o el fibrinógeno de la sangre.
Las proteínas se clasifican en dos grandes grupos
· Proteínas simples
· Proteínas conjugadas
Proteínas simples: son aquellas que por hidrólisis solo dan origen a aa. Pueden estar formadas por más de una cadena polipeptídica, por ejemplo albúminas, globulinas, histonas, glutelinas, escleroproteínas como queratina, colágeno, elastinas.Proteínas conjugadas: formadas por asociación de una proteína simple y una porción no proteica integrando una unidad molecular. Corrientemente se llama apoproteína a la porción proteica, mientras que la otra porción se denomina grupo prostético
La conformación que presenta una proteína va a depender directamente de los distintos niveles estructurales (hasta cuatro) que posee:
a) Estructura primaria: hace referencia a la posición que ocupa cada aminoácido en la cadena polipeptídica, es decir nos da idea de la secuencia de la proteína. La importancia de este nivel radica en que la posición que ocupa cada aminoácido dentro de la cadena va a condicionar enormemente el resto de los niveles estructurales y en último término la función que desempeña la proteína.
b) Estructura secundaria: hace referencia a la ordenación regular y periódica de la cadena polipeptídica en una dirección determinada. Básicamente, podemos encontrar dos tipos de estructura secundaria, la hélice-a y la conformación-ß.
En la Hélice-a (Fig.8) la cadena polipeptídica adopta una conformación helicoidal. Las estructuras helicoidales se caracterizan por el numero de aminoácidos por vuelta (n) y por su paso de rosca (p), o distancia entre vueltas. Esta conformación se estabiliza por puentes de hidrógeno (R-C=O ····· H-N-R) intracatenarios (dentro de la hélice). Además, los restos -R de los aminoácidos se disponen hacia fuera de la hélice evitando las interacciones estéricas (por grupos voluminosos) y estabilizando la conformación. Por otro lado, la hélice-a se distorsiona o pierde la conformación cuando en la secuencia aparece una prolina, único aminoácido ciclado por su grupo a-amino.
En la conformación-ß la cadena adopta una ordenación lineal en la que los restos -R, de los aminoácidos, se van alternando por encima y por debajo (zig-zag) del plano del enlace peptídico. Esta conformación se estabiliza con puentes de hidrógeno entre varias cadenas de proteínas con conformación-ß. El resultado de estas interacciones es la hoja plegada ß, que puede presentar un plegamiento paralelo, (en el que las cadenas vecinas se desarrollan en la misma dirección), o bien un plegamiento antiparalelo con cadenas vecinas en direcciones opuestas.
c)Estructura terciaria : hace referencia al modo en que se curvan o pliegan en el espacio los segmentos de hélice-a y/o conformación-ß, que presenta una cadena polipeptídica de los proteínas globulares.
d) Estructura cuaternaria: Muchas proteínas globulares son oligoméricas, es decir están formadas por más de una subunidad polipeptídica. La posición espacial que ocupa cada una de estas subunidades respecto a las otras queda determinada por la estructura cuaternaria.
AMINOACIDOS
1. Estructura y clasificación de los aminoácidos.
Como su nombre indica los aminoácidos son compuestos que poseen un grupo amino (-NH2) y un grupo ácido (carboxílico -COOH) en su estructura. Los aminoácidos son los precursores de los péptidos y las proteínas, y en ellos el grupo amino y el grupo carboxilo, se encuentran unidos al mismo átomo de carbono, conocido como carbono-a (a-aminoácidos).
La diferencia entre los aminoácidos viene dada por el resto -R, o cadena lateral, unida al carbono-a. Atendiendo a la naturaleza del grupo -R los aas pueden clasificarse en:
· Neutros o apolares
· Polares sin carga
· Polares con carga negativa
· Polares con carga positiva
Esta clasificación se ha realizado en base al grupo -R, pero es importante indicar que a pH fisiológico (pH 7,3), el grupo a-amino se encuentra cargado positivamente y el grupo a-carboxilo lo está negativamente.
Propiedades ácido-base
El pH del medio en el que se encuentre el aminoácido es esencial para determinar sus propiedades ácido-base, aspecto importante pues de ello dependen las propiedades químicas y la funcionalidad biológica de los péptidos y proteínas que forman.Las propiedades ácido-base de un aminoácido vienen determinadas por los grupos protonables que posea. Un aminoácido puede actuar bien como ácido o como base (sustancias anfóteras), pudiendo tener hasta tres grupos con carácter ácido-base: el a-amino, el a-carboxilo y, en algunos casos, el resto -R. Lo importante es que estos grupos poseen un carácter ácido-base débil, lo que hace que, dependiendo del pH, el correspondiente equilibrio pueda desplazarse en un sentido o en otro (hacia la forma protonada o hacia la desprotonada.
Como su nombre indica los aminoácidos son compuestos que poseen un grupo amino (-NH2) y un grupo ácido (carboxílico -COOH) en su estructura. Los aminoácidos son los precursores de los péptidos y las proteínas, y en ellos el grupo amino y el grupo carboxilo, se encuentran unidos al mismo átomo de carbono, conocido como carbono-a (a-aminoácidos).
La diferencia entre los aminoácidos viene dada por el resto -R, o cadena lateral, unida al carbono-a. Atendiendo a la naturaleza del grupo -R los aas pueden clasificarse en:
· Neutros o apolares
· Polares sin carga
· Polares con carga negativa
· Polares con carga positiva
Esta clasificación se ha realizado en base al grupo -R, pero es importante indicar que a pH fisiológico (pH 7,3), el grupo a-amino se encuentra cargado positivamente y el grupo a-carboxilo lo está negativamente.
Propiedades ácido-base
El pH del medio en el que se encuentre el aminoácido es esencial para determinar sus propiedades ácido-base, aspecto importante pues de ello dependen las propiedades químicas y la funcionalidad biológica de los péptidos y proteínas que forman.Las propiedades ácido-base de un aminoácido vienen determinadas por los grupos protonables que posea. Un aminoácido puede actuar bien como ácido o como base (sustancias anfóteras), pudiendo tener hasta tres grupos con carácter ácido-base: el a-amino, el a-carboxilo y, en algunos casos, el resto -R. Lo importante es que estos grupos poseen un carácter ácido-base débil, lo que hace que, dependiendo del pH, el correspondiente equilibrio pueda desplazarse en un sentido o en otro (hacia la forma protonada o hacia la desprotonada.
ÁCIDOS NUCLEICOS
Los ácidos nucleicos son polinucleótidos, es decir, polímeros resultantes de la unión mediante enlace fosfodiéster de un número variable de unidades monoméricas básicas, denominadas nucleótidos.
Un nucleótido está formado por tres componentes. Una pentosa, un compuesto heterocíclico nitrogenado (base nitrogenada) que junto con la pentosa forma un nucleósido, y una molécula de ácido fosfórico. Los nucleótidos tienen papeles muy variados dentro del metabolismo celular. Son la moneda energética en el metabolismo (ej: ATP), son mensajeros químicos secundarios en la respuesta celular a los estímulos inducidos por hormonas o agentes externos (ej.: AMPc), constituyen una serie de importantes cofactores enzimáticos y, por supuesto, son los constituyentes de los ácidos nucleicos: ribonucleicos (ARN) y desoxiribonucleicos (ADN).
NucleótidosLos nucleótidos son ésteres fosfóricos de los nucleósidos. Todos los nucleótidos naturales poseen el grupo fosfato unido al átomo de carbono 5' de la pentosa.
Un nucleótido está formado por tres componentes. Una pentosa, un compuesto heterocíclico nitrogenado (base nitrogenada) que junto con la pentosa forma un nucleósido, y una molécula de ácido fosfórico. Los nucleótidos tienen papeles muy variados dentro del metabolismo celular. Son la moneda energética en el metabolismo (ej: ATP), son mensajeros químicos secundarios en la respuesta celular a los estímulos inducidos por hormonas o agentes externos (ej.: AMPc), constituyen una serie de importantes cofactores enzimáticos y, por supuesto, son los constituyentes de los ácidos nucleicos: ribonucleicos (ARN) y desoxiribonucleicos (ADN).
NucleótidosLos nucleótidos son ésteres fosfóricos de los nucleósidos. Todos los nucleótidos naturales poseen el grupo fosfato unido al átomo de carbono 5' de la pentosa.
Suscribirse a:
Comentarios (Atom)